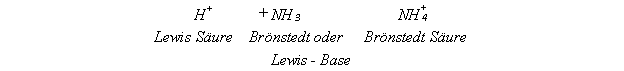Das Säure-Base Konzept von Lewis
Auch die Definition von Brönstedt war nicht in der Lage, alle
Beobachtungen zu erklären. So zeigen z.B Stoffe wie SO3, BF3 und AlCl3
beim  Auflösen
in Wasser eine saure Reaktion, obwohl sie keine wasserstoffhaltigen
Verbindungen sind. Auch aprotische Systeme waren nach Brönstedt bisher
noch nicht erfaßt. Aus diesem Grund schuf Lewis (1923, 1938) ein neues
Säure-Base Konzept, bei dem die Elektronenkonfiguration der teilchen
als konstitutionelles Merkmal in den Vordergrund rückte. Die
Definitionen lauten dann wie folgt:
Auflösen
in Wasser eine saure Reaktion, obwohl sie keine wasserstoffhaltigen
Verbindungen sind. Auch aprotische Systeme waren nach Brönstedt bisher
noch nicht erfaßt. Aus diesem Grund schuf Lewis (1923, 1938) ein neues
Säure-Base Konzept, bei dem die Elektronenkonfiguration der teilchen
als konstitutionelles Merkmal in den Vordergrund rückte. Die
Definitionen lauten dann wie folgt:
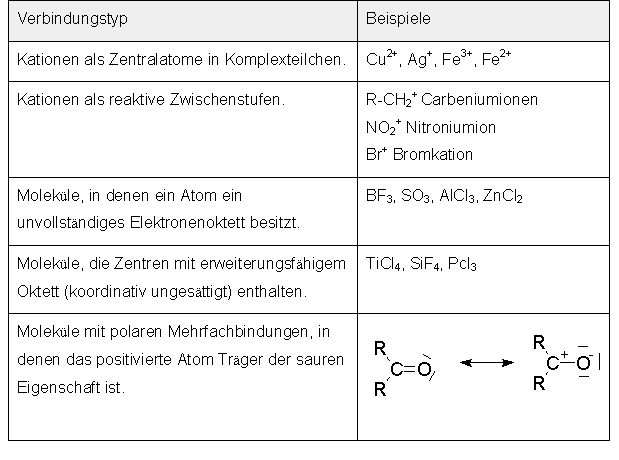
Lewis-Säuren sind Moleküle oder Ionen mit einer unvollständig besetzten
äußeren Elektronenschale (Teilchen mit Elektronenlücke), die gegenüber
anderen Teilchen unter Ausbildung einer kovalenten Bindung als
Elektronenpaarakzeptor wirken können.
Lewis-Basen sind Moleküle oder Ionen mit einem freien Elektronenpaar,
das zur Ausbildung einer kovalenten Bindung zur Vefügung gestellt
werden kann(Elektronenpaardonatoren).
 Mit
der Säure-Base Definition nach Lewis ist es nun z. B. auch möglich,
Komplexbildungsreaktionen als Säure-Base Reaktionen aufzufassen.
Mit
der Säure-Base Definition nach Lewis ist es nun z. B. auch möglich,
Komplexbildungsreaktionen als Säure-Base Reaktionen aufzufassen.
Weiterhin wird durch die Definition nach Lewis eine Trennung von den
Protonensäuren vorgenommen, d. h. Es können eine Vielzahl von
Verbindungen als Lewis-Säuren reagieren.
Die Brönstedtsche Protonensäuren stellen nach der Definition von Lewis
keine Säuren dar. Betrachtet man das Proton jedoch als Lewis- Säure, so
ist die Bildung einer Brönstedt- Säure eine Lewis Säure- Base Reaktion.
Als Lewis- Basen (welche zugleich auch Brönstedt Basen sind) reagiern:
*Moleküle mit besetzten Orbitalen, die nicht in einer Atombindung
beansprucht sind.
*Anionen als Komplexliganden.
*Moleküle mit polaren Mehrfachbindungen, in denen das negativierte Atom
Träger der basischen Eigenschaften ist.
Vorteile des Lewis'schen Säure-Base Konzeptes:
*konstitutionelles Merkmal der Lewis-Säuren und -Basen ist die
Elektronenkonfiguration.
*Komplexbildung wird als neutralisationsanolger Prozeß beschrieben!
*Stärke Erweiterung des Säure-Begriffes
Nachteile der Definition nach Lewis:
*Brönstedt-Säuren nehmen eine Sonderstellung ein
*Kaum zur quantitativen Beschreibung der relativen Stärke eine Säure
bzw. Base geeignet. Damit ist auch keine quantitative Beschreibung von
Säure-Base Gleichgewichten möglich.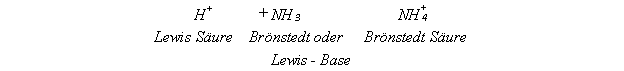
 Auflösen
in Wasser eine saure Reaktion, obwohl sie keine wasserstoffhaltigen
Verbindungen sind. Auch aprotische Systeme waren nach Brönstedt bisher
noch nicht erfaßt. Aus diesem Grund schuf Lewis (1923, 1938) ein neues
Säure-Base Konzept, bei dem die Elektronenkonfiguration der teilchen
als konstitutionelles Merkmal in den Vordergrund rückte. Die
Definitionen lauten dann wie folgt:
Auflösen
in Wasser eine saure Reaktion, obwohl sie keine wasserstoffhaltigen
Verbindungen sind. Auch aprotische Systeme waren nach Brönstedt bisher
noch nicht erfaßt. Aus diesem Grund schuf Lewis (1923, 1938) ein neues
Säure-Base Konzept, bei dem die Elektronenkonfiguration der teilchen
als konstitutionelles Merkmal in den Vordergrund rückte. Die
Definitionen lauten dann wie folgt: Mit
der Säure-Base Definition nach Lewis ist es nun z. B. auch möglich,
Komplexbildungsreaktionen als Säure-Base Reaktionen aufzufassen.
Mit
der Säure-Base Definition nach Lewis ist es nun z. B. auch möglich,
Komplexbildungsreaktionen als Säure-Base Reaktionen aufzufassen.